【前回記事を読む】A氏の発見は学会でも高く評価されたが…余韻は長く続かなかった。論文発表から数週間後、ある疑問がA氏に迫り結局…
第1章 創薬ベンチャーの現状と課題
――日本と世界の比較から見える壁
国の狙いは明快です。創薬ベンチャーを育てることは、単に企業数を増やすことではありません。人々に新しい治療法を届け、日本発の技術を世界に広げ、医療と産業の未来を切り拓くことにつながるのです。だからこそ、創薬ベンチャーは今、国の成長戦略においても特別な位置を与えられているのです。
ただし、多くの創薬ベンチャーはまだ安定した収益源を持たず、研究・開発費用の大部分を外部資金に依存しています。そのため各国では、産業育成を目的とした資金援助制度が整備されています。
しかし日本では、質の高い研究シーズやiPS細胞に代表される革新的な基盤技術があるにもかかわらず、創薬ベンチャーの数は欧米に比べて少数にとどまります。米国に数千社規模のバイオベンチャーが存在するのに対し、日本は数百社程度です。その背景には、開発の長期化や高コストに加え、日本特有の構造的な課題があります。
最大の障壁の一つは、アカデミアで生まれた研究成果が事業化に至るまでの資金不足、いわゆる「死の谷」です。特に概念実証(Proof of Concept,PoC:「概念実証:研究段階の技術が臨床や事業で実現可能かを示す証拠」)段階を乗り越えるための初期資金が不足し、多くの有望な技術が社会実装に結びつかない事態が起こっています。
たとえばGAPファンドは、大学や研究機関で生まれた研究成果を事業化につなげる「橋渡し資金」として重要な役割を果たしています。数百万円規模の初期実験支援から、数千万円〜1億円規模の臨床準備まで、段階的に研究成果を育てる仕組みとなっており、研究シーズが「死の谷」を越える足場となっています。
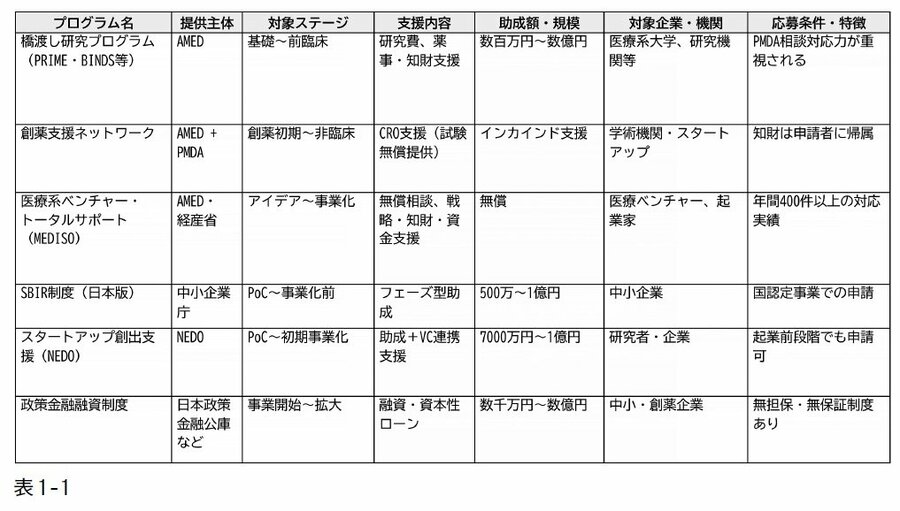
名古屋大学を中心に展開するTongali GAPファンド、東京大学や京都大学の独自ファンドなど、全国各地でこの仕組みが広がっています。表1-1に、日本の主要プログラムを一覧化しました。
海外の制度も見てみましょう。米国のバイオ医薬品支援は、NIHのSBIR/ STTRとBARDAの二本柱で成り立っています[1][2]。SBIR/STTRはフェーズごとに数十万〜数百万ドル規模の競争的助成金を提供し、技術の実現可能性検証から商業化に向けた開発継続まで段階的に支援します。一方、
BARDAはパンデミックなど国家的ニーズに直結する開発を対象に、数千万〜数億ドル規模の巨額資金を投じ、柔軟な契約形態で後期開発から備蓄までを加速します。